- سفير اليمن يبحث مع وزيرة التعليم الجزائرية تعزيز التعاون في مجال التعليم الفني والتدريب المهني
- البرهان: الانسحاب من الفاشر ضروري وسنقتص لأهاليه
- "جئتُ لأُفضفض لكم".. أب من غزة لا يزال يبحث عن جثث عائلته تحت الأنقاض
- وزير الشباب والرياضة يناقش برامج تأهيل وتدريب شباب الضالع واوضاع نادي عرفان ابين
- تدشين اولى رحلات شركة طيران عدن
- وزير الأوقاف والإرشاد يترأس اجتماعاً للجنة المناقصات والمزايدات
- اليمن يشارك في المسابقة العالمية للروبوت والذكاء الاصطناعي في بنما
- "لا نريد رؤيتها".. نيكي نيكول تُغضب عائلة لامين يامال
- الكرملين: اختبار الصاروخ النووي يعكس مخاوف أمنية روسية
- اليوم التالي في غزة.. هل يتدارك نتنياهو "الفشل الاستراتيجي"؟
- لغز عمره ربع قرن.. اكتشاف يغير فهم العلماء لتضاريس المريخ
- بعد زوجته.. نجل مروان البرغوثي يوجه رسالة إلى ترامب
- المرشح لرئاسة لجنة إدراة غزة.. من هو أمجد الشوا؟
- حماس تتحدث عن عوائق: مَنْ دفنوا الجثث المتبقية قتلوا بالحرب
- غزة بعد الاتفاق.. شهيدان بغارة للاحتلال والقسام تنتشل جثمان أسير إسرائيلي
- "قنبلة موقوتة".. عشرات الناقلات من الأسطول الشبح الروسي بخليج فنلندا
- أردوغان وستارمر يؤكدان ضرورة الحفاظ على وقف إطلاق النار بغزة
- تركيا تشتري 20 مقاتلة "تايفون" من بريطانيا.. ماذا تعرف عنها؟
الإنسولين.. من الاستخراج من الأبقار إلى التصنيع عبر البكتيريا
في حال واجهت مشكلة في مشاهدة الفيديو، إضغط على رابط المصدر للمشاهدة على الموقع الرسمي
في ديسمبر/كانون الأول 1921 كان ليونارد طومسون البالغ من العمر 14 عاما على وشك الموت.
كان الصبي مصابا بداء السكري ووزنه 65 رطلا فقط، وبعد شهر في مستشفى تورنتو العام لم تتحسن حالته، لذا لجأ أطباؤه إلى علاج تجريبي قيد التطوير من قبل باحثين كنديين.
وفي يناير/كانون الثاني 1922 حقن الأطباء طومسون بحذر بسائل بنكرياسي مستخرج من الأبقار، كان الفهم العلمي والطبي لداء السكري غامضا في ذلك الوقت، ولكنه كان يتقدم بسرعة.
ومن خلال حقن الصبي كان أعضاء الفريق يأملون في تأكيد ما شاهدوه بالفعل في الحيوانات، شيء مستخرج من بنكرياس سليم ينظم سكر الدم، وكان لدى العلماء اسم لهذا الشيء الغامض: الإنسولين.
وكما اتضح، أنقذت الحقنة حياة طومسون، مما مثل نقطة تحول في علاج حالة كانت حتى ذلك الحين بمثابة حكم إعدام فعلي، وذلك وفقا للجمعية الكيميائية الأميركية (إيه سي إس إيه سي إس).
داء السكري مرض مزمن يعطل آلية استقلاب الجسم سكر الدم، وعادة ما يشير ارتفاع نسبة السكر في الدم إلى إفراز البنكرياس الإنسولين.
لكن في أحد أشكال داء السكري -وهو النوع الأول- نعلم الآن أن البنكرياس ينتج القليل من الإنسولين أو لا ينتجه على الإطلاق، وفي النوع الثاني قد ينتج البنكرياس الإنسولين ولكن لا يستطيع الجسم استخدامه بفاعلية.
وفي كلتا الحالتين، ترتفع مستويات الغلوكوز في الجسم، مما يؤدي في النهاية إلى مشاكل خطيرة في الدورة الدموية والجهاز العصبي والجهاز المناعي، وبالتالي يمكن أن يؤدي ذلك إلى العمى أو قصور الكلى أو القلب أو السكتة الدماغية.
وعلى الرغم من التقدم المحرز منذ عهد طومسون فإن داء السكري لا يزال هو السبب التاسع الرئيسي للوفاة في جميع أنحاء العالم، حيث توفي 1.5 مليون شخص بسبب المرض في عام 2019.
ويتزايد العبء العالمي لداء السكري، فقد كان هناك 108 ملايين شخص مصابين بداء السكري في عام 1980، ولكن هذا العدد ارتفع إلى 422 مليونا بحلول عام 2014، وفقا لمنظمة الصحة العالمية.
ومع ذلك، بالنسبة لأولئك الذين يمكنهم الوصول إلى الإنسولين أصبح داء السكري الآن حالة يمكن التحكم فيها إلى حد كبير.
ويواصل الباحثون في علم الأدوية كشف غموض مرض السكري، لقد تعلموا فهم طبيعة المرض وكيفية السيطرة عليه وكيفية إعداد العلاجات وتحسينها، وبذلك أنقذوا ملايين الأرواح، ولا تزال قصة النجاح والتحسن المستدام مستمرة حتى اليوم.
ما وظيفة جرعة الإنسولين؟
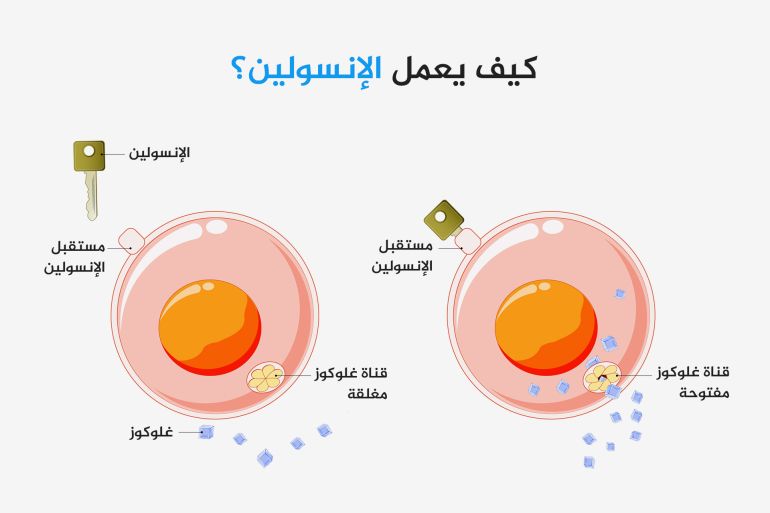
ينظم هرمون الإنسولين تركيزات الغلوكوز في الدم، وهو السكر الذي ينتجه الجسم عند هضم الطعام، ولأن الجسم يستقلب الإنسولين فإنه يجب عليه تجديد مخزونه بانتظام، إما عن طريق البنكرياس أو في حالة مرضى السكري عن طريق الحقن.
في البنكرياس وفي حقن مرضى السكري يكون الإنسولين في صورة غير نشطة تسمى "سداسي الإنسولين"، وعلى المستوى الجزيئي فإن سداسي الإنسولين هو كرة من 6 جزيئات إنسولين متصلة ببعضها البعض.
لا تستجيب الخلايا للإنسولين بهذا الشكل الكبير والمتناسق، ولكن في الجسم يتحلل سداسي الإنسولين بشكل طبيعي إلى مكوناته أو المونومرات، لهذا السبب تكون نظائر الإنسولين التي تؤخذ مع الوجبات أسرع في المفعول، فهي تصل إلى شكل المونومرات بشكل أسرع.
وترتبط مونومرات الإنسولين بمستقبلات البروتين على السطح الخارجي للخلايا، مما يحفز تغييرا هيكليا ينتشر عبر الغشاء، وهذا التأثير المتتالي يحفز الخلايا على امتصاص المزيد من الغلوكوز، مما يقلل مستويات الغلوكوز المتداولة في مجرى الدم.
التاريخ المبكر
يمتد التاريخ المسجل لمرض السكري إلى 3500 عام، إلى بردية مصرية وثق فيها الطبيب هسي رع حالة "كثرة التبول"، نعلم الآن أنه عندما لا تتمكن الكلى من تصفية ما يكفي من الغلوكوز الزائد من الدم فإنها تطلق المزيد من السوائل السكرية في البول.
تم الحصول على مزيد من المعرفة في عام 1675 عندما تذوق الطبيب البريطاني توماس ويليس بول مرضاه، إذا كان طعم بولهم حلوا فقد شخّص إصابتهم بداء السكري، ولا يزال أحد الاختبارات الحالية يتحقق من مستوى السكر في البول، ولكنه لم يعد يعتمد على تذوقه.
وبعدما يقارب 200 عام -وتحديدا في عام 1869- لاحظ طالب الطب الألماني بول لانغرهانز أن البنكرياس يحتوي على "جُزر" من نوع مميز من الخلايا على الرغم من أنه لم يكن يعرف وظيفتها.
وبعد بضعة عقود أظهر الباحثون أن إزالة البنكرياس من كلب تسبب مرض السكري، وخلصوا إلى أن البنكرياس ينتج مادة ضرورية لاستقلاب السكر.
وفي عام 1909 تم تقديم مصطلح الإنسولين، وهو مشتق من الكلمة اللاتينية التي تعني جزيرة، ويشير الإنسولين إلى المادة الافتراضية التي تنتجها خلايا "جزيرة" البنكرياس الخاصة بلانغرهانز.
ومن أوائل الأدلة التي تدعم نظرية الإنسولين أن خلايا لانغرهانز وجد أنها مدمرة لدى مرضى السكري من النوع الأول.
ثم في عام 1916 أظهر عالم وظائف الأعضاء الروماني نيكولاس باوليسكو من جامعة بوخارست أن مستخلصا من خلايا البنكرياس يخفض سكر الدم لدى الكلاب المصابة بالسكري.
كما عمل باحثون آخرون على مستخلصات، لكن محاولات استخراج الإنسولين بدت إما أنها تدمر المادة الفعالة أو تلوث المنتج بشوائب سامة، مما يمنع استخدام هذا المنتج المحتمل.
بانتينغ
ألهمت هذه التحديات الطبيب الكندي فريدريك بانتينغ لإجراء تجاربه الخاصة بدءا من عام 1921.
عمل بانتينغ مع تشارلز بيست وجيمس كوليب بتوجيه من أستاذ علم وظائف الأعضاء في جامعة تورنتو جون جيمس ريكارد ماكلويد، وابتكر الفريق عملية لاستخراج مستخلص من خلايا البنكرياس وتنقيته على شكل إنسولين.
وتضمن أحد أهم إنجازاتهم الاستخلاص باستخدام نحو 90% من الكحول، والذي أذاب الإنسولين بشكل انتقائي بحيث يمكن فصله عن بعض الشوائب.
وبعد نجاح اختبار حقن الإنسولين في الكلاب والأرانب أصبح العلاج جاهزا للتجارب البشرية بدءا من ليونارد طومسون في يناير/كانون الثاني 1922.
وخفضت التجربة نسبة السكر في دمه إلى مستويات قريبة من الطبيعية وأنقذت حياته.
قام أعضاء فريق جامعة تورنتو بتحسين عملية الإنتاج الخاصة بهم عن طريق استخراج أنسجة البنكرياس أولا في الأسيتون المحمض قليلا، متبوعا باستخراج الكحول.
كان الأطباء الذين سمعوا عن الدواء الجديد العجيب يطالبون بشدة بالحصول على الإنسولين لإنقاذ مرضاهم المحتضرين، لكن الجامعة لم تتمكن من إنتاج كميات كبيرة.
وفي مايو/أيار 1922 بدأت شركة الأدوية إيلي ليلي وشركاها التعاون مع الجامعة لتوسيع نطاق إنتاج الإنسولين وتسويقه في الأميركتين، وقاد هذا الجهد الكيميائي جورج والدن من شركة ليلي.
وبحلول يوليو/تموز شحنت الشركة أولى دفعاتها من إنسولين إليتين للاختبارات السريرية.
وبين عشية وضحاها تقريبا غيّر علاج مستخلص البنكرياس الحيواني مرض السكري من حالة مميتة.
عاش تومسون حتى سن الـ26، وعاش أطفال آخرون من تلك السنوات الأولى من العلاج الرائد لفترة أطول.
توفيت إليزابيث هيوز -وهي واحدة من أوائل الأشخاص الذين عالجهم بانتينغ بالإنسولين- عن عمر يناهز 73 عاما بعد أن تلقت ما يقارب 42 ألف حقنة إنسولين على مدار 58 عاما.
وفي عام 1923 -وهو العام الذي تلا التجربة السريرية- حصل بانتينغ وماكلويد على جائزة نوبل لاكتشاف الإنسولين.
كان تأثير الإنسولين مذهلا للغاية نظرا لتأثيره المذهل على مرضى السكري، أولئك الذين شاهدوا أول مرضى السكري الذين كانوا يتضورون جوعا وأحيانا في غيبوبة وهم يتلقون الإنسولين ويعودون إلى الحياة شهدوا إحدى معجزات الطب الحديث الحقيقية.
الإنسولين الصناعي
بدأ الإنتاج الضخم للإنسولين المستخرج من الحيوانات في أعقاب التجارب السريرية الناجحة في تورنتو وأماكن أخرى عام 1922، وبالإضافة إلى ليلي بدأت جهات أخرى في إنتاج الإنسولين، بما في ذلك مختبر نورديسك للإنسولين غير الربحي الذي أصبح لاحقا نوفو نورديسك، وشركة هوكست إيه جي التي سبقت سانوفي.
كانت القدرة على إنتاج منتج نقي وقابل للتكرار ذات أهمية بالغة لشركات الأدوية التي تتطلع إلى توسيع نطاقها، وقد أشارت التجارب المبكرة للأطباء إلى أن نقاء المستخلص يؤثر على نتائج المرضى، لذلك سعى الكيميائيون إلى تطوير طرق جديدة لتنقية "الدواء المعجزة".
تم تحقيق إنجاز مهم بفضل التقدم في تقنية تُعرف باسم "الترسيب الكهربائي المتساوي"، والتي تم اكتشافها بشكل مستقل في ليلي وجامعة واشنطن في سانت لويس.
وتحتوي مستخلصات البنكرياس على العديد من البروتينات المختلفة، ولكل منها أحجام جزيئية مختلفة وخصائص كيميائية وشحنات كهروستاتيكية، ويؤدي تعديل الرقم الهيدروجيني للمحلول الذي يحتوي على الخليط إلى تغيير شحنة تلك البروتينات، مع استجابة أنواع مختلفة من البروتينات عند درجة حموضة مختلفة.
وعند درجة حموضة معينة تصبح بعض البروتينات متعادلة، مما يؤدي إلى ترسبها خارج المحلول لسهولة عزلها، في حين تظل الملوثات غير المرغوب فيها مذابة.
وفي عام 1923 بدأت شركة ليلي إنتاج الإنسولين الحيواني على نطاق واسع بناء على تقنية الفصل هذه، وأحدث هذا ثورة في نقاء واستقرار المنتج النهائي، مما مهّد الطريق للإنتاج الضخم.
وعلى مدى العقود التالية تعلّم الباحثون المزيد عن المستخلص الذي لا يزال غامضا، ولطالما اعتُبر الإنسولين مزيجا من البروتينات، ولكن ابتداء من عام 1924 ظهرت أدلة على أن الإنسولين قد يكون بروتينا واحدا، وأثبت علماء من جامعة جونز هوبكنز هذه الفرضية في عام 1935.
ثم، بين عامي 1951 و1955 حدد عالم الكيمياء الحيوية الإنجليزي فريدريك سانجر تسلسل الأحماض الأمينية لهذا البروتين الواحد، وأثرت هذه الاكتشافات على نظرة العالم للإنسولين، ولعل الأهم من ذلك هو أنها حفزت العلماء على تخيل كيفية تنقية الإنسولين، بل وتصنيعه بأنفسهم.
تحديث الإنسولين
أثبت النظر إلى الإنسولين ككيان كيميائي واحد بدلا من مستخلص غير متجانس أنه أمر أساسي لتحسين إمكانياته كدواء بشكل جذري، وتمكن العلماء من تطبيق قواعد الكيمياء لتنقية جزيء الإنسولين بشكل أفضل.
بدأت شركات الأدوية في الوصول إلى نقاء يتراوح بين 80 و90% بحلول سبعينيات القرن الماضي باستخدام تقنيات مثل الكروماتوغرافيا.
والأهم من ذلك أنها امتلكت أيضا الأدوات اللازمة لتحديد التركيب الدقيق لجزيئات الإنسولين.
وعلى سبيل المثال، اكتشف الباحثون أن الإنسولين يتكون من سلسلتين طويلتين من الأحماض الأمينية (سلاسل بولي ببتيد) يطلق عليهما "إيه" و"بي"، وتربطهما "جسور" تحتوي على الكبريت.
لكن ليس كل الإنسولين متساويا، فالإنسولين البشري يختلف عن إنسولين البقر الذي يختلف بدوره عن إنسولين الخنزير، ويحتوي كل منهما على سلاسل مكافئة إلى حد كبير من وحدات بناء الأحماض الأمينية مع بعض التغييرات التي تحددها منفصلين.
وحتى ثمانينيات القرن الماضي كان الأطباء يعالجون مرض السكري لدى البشر باستخدام الإنسولين المستخرج من الحيوانات، خاصة الخنازير والأبقار.
لكن في أعقاب ثورة التكنولوجيا الحيوية الناشئة بدأ ذلك أيضا في التغير، حيث سعى المصنعون إلى تجنب الإمكانيات المسببة للحساسية لهذه المنتجات الحيوانية، وتعاون خبراء تحرير الحمض النووي في جينينتك مع شركة ليلي لتطوير عملية جديدة تستخدم الميكروبات لإنتاج الإنسولين.
تخيل أي خلية ميكروبية كنوع من مصنع البروتين: تصنع كل خلية البروتينات بشكل طبيعي بناء على التعليمات المكتوبة في حمضها النووي.
عرف كيميائيو الأدوية البروتين الذي يريدونه، وصولا إلى كتلة بناء الأحماض الأمينية الفردية، وقد أتاحت أدواتهم الجديدة إمكانية خياطة التعليمات الجينية المخصصة في مخططات الحمض النووي للميكروبات.
استخدم المتعاونون عملية "الحمض النووي المؤتلف" هذه لإنتاج الإنسولين البشري من البكتيريا بنسبة نقاء 98%، وفي عام 1982 وافقت إدارة الغذاء والدواء على الدواء الناتج "هومولين" (Humulin).
قدّم نجاح "هومولين" حجة قوية لدور الهندسة الوراثية الجديد في الكيمياء الصيدلانية، فقد أصبحت للكيميائيين الآن سيطرة شبه كاملة على تسلسل الأحماض الأمينية لمنتجاتهم، ويمكنهم الوصول إلى درجات نقاء أعلى.
وفتح هذا الباب أمام العلماء الذين يتطلعون إلى تعديل الدواء الذي لا يزال غير مثالي وضبطه.
المستقبل التناظري
تعتمد وظيفة البروتين على تركيبه الكيميائي، ويؤثر حجم وشحنة ونوع العناصر المرتبطة بكل حمض أميني على خصائص البروتين الرئيسية التي تؤثر على السمات الصيدلانية: كيفية معالجة الخلايا للدواء ومدى استقرار الجزيء ومدى فعاليته.
لذلك، بدأ باحثو الأدوية مسلحين بأدوات التخصيص الإضافية للهندسة الوراثية اختراع "نظائر" الإنسولين، وهي أشكال مختلفة من بروتين الإنسولين الطبيعي تهدف إلى تعزيز الأداء.
وفي هذه الحالة، لا يعني تعزيز الأداء مجرد زيادة الفعالية، بل هو أيضا طريقة للتغلب على مشكلة الجرعة، فإذا كانت جرعة الإنسولين لدى الشخص منخفضة جدا فلن يحصل على فائدة كافية، وإذا كانت جرعته عالية جدا فإن الإنسولين الزائد يخاطر بإزالة الكثير من الغلوكوز في الدم والتسبب في نقص سكر الدم بشكل خطير، وإن "نافذة" الجرعة العلاجية للإنسولين الطبيعي ضيقة بشكل غير مريح.
وللتغلب على مشاكل الجرعة قام العلماء بضبط بنية الإنسولين من خلال العبث بالأحماض الأمينية الفردية للبروتين، ويتم ذلك عن طريق تبديل ترتيب بعض الأحماض الأمينية أو إضافة أو حذف بعضها مثل تغيير الخرز في قلادة.
ويؤدي تبديل الترتيب إلى تغيير خصائص الإنسولين، فعلى سبيل المثال يتحلل ليسبرو -وهو نظير من إنتاج شركة ليلي- من مجمعات كبيرة إلى وحدات فرعية صغيرة بسرعة أكبر من الإنسولين العادي، مما يعني أنه يصبح متاحا للخلايا بشكل وتوافر أسرع، وهو مفيد لجرعة وقت الوجبة، ويقلل احتمالية نقص سكر الدم الناتج عن بقاء الإنسولين، ويعتمد إنسولين أسبارت من نوفو نورديسك على مبدأ مماثل.
وهناك نهج مختلف يتضمن تغيير بعض الأحماض الأمينية لإنتاج نظائر أكثر استقرارا وطويلة الأمد للاستخدام الأساسي للإنسولين مرة واحدة يوميا.
وقد ابتكرت "نوفو نورديسك" إنسولين ديجلوديك بهذا النهج، في حين استخدمته شركة أفينتيس -التي أصبحت جزءا من سانوفي- لإنتاج إنسولين غلارجين.
إن التغييرات الطفيفة في ديجلوديك وغلارجين تجعل الجزيئات أقل قابلية للذوبان، لذا تذوب في مجرى الدم ببطء دون التسبب في ارتفاعات سريعة في مستويات الإنسولين.
والهدف الشامل هو زيادة الإنسولين في الدم عند الحاجة إليه، وتقليله عند عدم الحاجة إليه.
ويفكر الباحثون من شركات الأدوية والشركات الناشئة الآن فيما يتجاوز التركيب الجزيئي والهندسة الوراثية، وقد تطلّع البعض إلى تقنيات مثل الإبر الدقيقة لحل مشكلة الجرعة.
يتم إنتاج الإنسولين بأشكال مختلفة لتلبية الاحتياجات المتنوعة لمرضى السكري، فالتركيبات سريعة المفعول تجعل الإنسولين متاحا للخلايا بشكل أسرع، في حين تطلق التركيبات طويلة المفعول الإنسولين بشكل أبطأ، مما يسمح لها بالتحكم في مستوى الغلوكوز لفترة أطول.
 المصدر:
الجزيرة
المصدر:
الجزيرة